Groult Hugo

- Équipe de rattachement : BCBS
- Statut : Chercheur
- hugo.groult*at*univ-lr.fr
- Curriculum vitae (PDF)
- Tél. : +33(O)5 46 50 76 74
Chercheur CRCN CNRS
Formation d’origine
Docteur en chimie pharmaceutique
(Programme Européen Marie Curie)
Ingénieur chimiste diplômé de
l’Ecole Nationale Supérieure de Chimie de Lille
Section de Recherche : CNRS sections 16
Institut référent : INC
Mots clés :
Nanomédecine : Nanoparticules d’oxyde de fer extrêmement petites ; Diagnostic par contraste positif en IRM ; Synthèse micro-onde ; Imagerie bimodale PET/IRM
Chimie carbohydrate : Polysaccharides sulfatés d’origine algale ; Carraghénane ; Héparine ; Dysfonctionnements enzymatiques, Propriétés anticoagulantes
Biologie cellulaire : Cancer ; Microenvironnement tumoral ; Heparanase ; Angiogenèse
Collaborations :
J. Ruiz-Cabello CIC biomaGUNE, Sàn Sebastian

C. Grillon Centre de Biophysique Moléculaire - UPR 4301

Financement
Région Nouvelle Aquitaine et Ligue contre le Cancer
Encadrement scientifique d’étudiants (Doctorants / Master 1 et 2)
- MANSEUR Chanez, (Thèse en cours, 2020-2023) : « Conception et optimisation d’oligosaccharides marines sulfatés pharmacomodulateur de la progression tumorale »
- COUSIN Rémi, (Thèse en cours, soutenance prévue décembre 2020) : Biochimie, Université de La Rochelle. « Développement de modèles cellulaires et d’outils moléculaires dédiés au suivi de l’inhibition ciblée de l’héparanase, une glycosidase impliquée dans les processus metastatiques et angiogéniques ». Direction : T. Maugard et I. Arnaudin
- MAURA Maheva, (Stage Master 2, 2017) : Biochimie, Université de La Rochelle. « Activités biologiques de nanovecteurs fonctionnalisés avec des dérivés de polysaccharides sulfatés anti-angiogéniques ».
Thèmes de Recherche.
Intervenant aux projets : COUSIN Rémi (Doctorant) ; Ferru-Clément Romain (ATER) ; Prunier Grégoire (IR, accompagnement technique biologie cellulaire) ; Chanez Manseur (Doctorante) ; Thierry Maugard (Enseignant-chercheur) ; Ingrid Arnaudin (Enseignante-chercheuse), Kevin Barranger, Pierre-Edouard Bodet (IE, accompagnement technique chimie analytique)
Activités pédagogiques
TP Nanobiotechnologies et outils optiques, Niveau M2
Liste des publications :
2026
Article dans une revue
2025
Article dans une revue
2024
Article dans une revue
2023
Article dans une revue
2022
Article dans une revue
2021
Article dans une revue
2020
Article dans une revue
2019
Article dans une revue
2018
Article dans une revue
2017
Article dans une revue
2014
Article dans une revue
2011
Article dans une revue
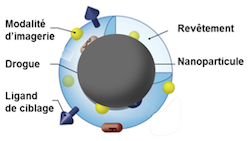
Du fait de leurs tailles, les nanoparticules présentent des propriétés physicochimiques uniques et se situent à la frontière entre l’échelle moléculaire et cellulaire. Elles peuvent ainsi afficher un caractère multifonctionnel en leurs associant plusieurs biomolécules qui assurent différentes actions biologiques spécifiques. En nanomédecine, les nanoparticules sont notamment utilisées pour la vectorisation ciblée d’actifs avec possibilité de libération contrôlée et le diagnostic par imagerie clinique. Parmi la large famille des nanomatériaux, les nanoparticules d’oxyde de fer (IONPs), du fait de leurs propriétés magnétiques singulières et bonne biocompatibilité, ont été largement proposées comme agents de contraste négatif pour l’imagerie par résonance magnétique (IRM), nano-transporteurs de molécules bioactives et dans des applications d’hyperthermie.

Néanmoins, les passages à la clinique sont rares et surtout l’utilisation des IONPs comme agent de contraste négatif en IRM est continuellement débattue (diagnostic difficile, images altérées, signaux endogènes) face aux agents de contraste positif bien plus favorables à la pratique clinique. De récents progrès ont toutefois réussi à obtenir un contraste positif approprié à l’imagerie IRM en utilisant des noyaux d’oxyde de fer extrêmement petits (< 5 nm) et des séquences IRM adaptées. Nous inscrivons nos recherches dans cette nouvelle génération d’IONPs qui pourrait représenter une remarquable alternative aux désavantages des chélates de gadolinium (Gd)-les agents de contraste positif les plus répandus. Les atouts apportés sont spécialement un long temps de vie vasculaire pour des acquisitions IRM prolongées plus précises, moins de toxicité et une possible multifonctionnalité (ciblage, bioactivité et imagerie multimodale).
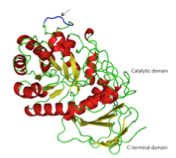
Actuellement, une recherche importante se porte sur les spécificités physicochimiques des microenvironnements tumoraux, notamment la surexpression d’enzymes hydrolytiques, comme nouveaux outils biologiques pour la mise en place de thérapie ciblée. La recherche en oncologie de ces dernières années a vu émerger une nouvelle cible qu’est l’héparanase (HPSE), un excellent biomarqueur pour de nombreuses pathologies. Cette glycosidase est la seule enzyme connue capable de cliver sélectivement l’héparane sulfate composante des protéoglycanes de la matrice extracellulaire. Elle participe ainsi au remodelage de la matrice et à la dégradation de la membrane basale vasculaire, permettant l’invasion et la migration des cellules cancéreuses. Elle contrôle également la libération de nombreuses molécules signales, séquestrées par la matrice, qui déclenchent des voies métaboliques favorisant notamment l’angiogenèse. L’inhibition spécifique de HPSE est donc considérée actuellement comme une nouvelle stratégie thérapeutique très séduisante.
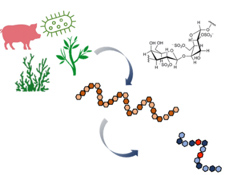
Parmi les différents inhibiteurs proposés, la classe des polysaccharides sulfatés a attiré une attention toute particulière en tant que mime structural de l’héparane sulfate, le substrat naturel de HPSE. Leur utilisation a toutefois longtemps été limitée du fait de leurs hauts poids moléculaires, complexités structurales et multiples bioactivités pouvant produire des effets secondaires. Cependant, des avancées récentes ont permis l’obtention de polysaccharides ou oligosaccharides sulfatés modifiés présentant des activités anti-HPSE plus spécifiques. Les synthèses utilisent des processus de dépolymérisation et/ou modifications chimiques. Ces stratégies ont notamment été appliquées à l’héparine, un standard de référence dans l’inhibition de HPSE mais qui présentait des propriétés anticoagulantes non-voulues. Bien que ces dérivés d’héparines fournissent actuellement deux des quatre composés en phase II/III d’essais cliniques, plusieurs obstacles restent à franchir. D’une part les mécanismes d’action à l’échelle moléculaire et la relation structure/fonction anti-HPSE des oligosaccharides n’est pas totalement élucidée. D’autre part, dans le cas des héparines, leurs productions d’origine animale avec des procédés de purification complexes et à faible rendement posent questions (coût économique, contamination possibles, impact environnemental). Dans ce contexte de recherche, nous poursuivons le criblage d’autres candidats polysaccharidiques en alternative, notamment d’origine algale ou bactérien.
Curieusement, HPSE n’est que très peu associée à des approches de nanomédecine. Outre son caractère de cible thérapeutique qui peut être visée par des nano-objets, ses utilisations potentielles comme outil biologique pour l’accumulation ciblée de sondes theragnostiques ou la libération contrôlée d’actifs apparaissent comme particulièrement séduisantes. De plus, les polysaccharides sulfatés –une classe des inhibiteurs de HPSE- sont déjà amplement utilisés dans la formulation des nano-objets. Néanmoins, ils sont principalement incorporés en tant que revêtements stabilisateurs charpentes pour améliorer la stabilité colloïdale, la bio-acceptabilité et la facilité de fonctionnalisation de nano-transporteurs chargés de convoyer une molécule bioactive exogène. Etonnamment, peu d’études décrivent des nano-objets fonctionnalisés avec des polysaccharides ou oligosaccharides sulfatés considérés comme le groupement fonctionnel principal de ciblage ou bien le principe bioactif à part entière. Ce constat général est en particulier frappant en ce qui concerne les nouvelles espèces polysaccharidiques spécifiquement anti-héparanase (dont celle évaluées en phases cliniques) qui n’ont pas encore été associées à un nano-objet.

Notre projet de recherche propose donc la conception de Nanovecteurs d’oxyde de fer fonctionnalisés par des polysaccharides sulfatés inhibiteurs de l’héparanase pour des applications thérapeutiques et diagnostiques par contraste positif en IRM. Cela permet de proposer une formulation originale dans laquelle les polysaccharides jouent un rôle « 3 en 1 » de i) revêtement pour garantir la stabilité colloïdale des nanoparticules, ii) ligand de ciblage pour l’accumulation des nanoparticules dans les tissus tumoraux sur-exprimant HPSE grâce à une interaction préférentielle substrat polymérique/enzyme et iii) molécule bioactive (inhibition résultante de l’enzyme). Ce concept original favorisera répond au principe de recherche « bench to bed » et repose sur la formulation originale d’agents biologique voisins d’entités déjà utilisées en clinique. Cela représente une alternative à la méthodologie « classique » de synthèse séquentielle des nanovecteurs multifonctionnels (fonctionnalisation étape par étape) qui peut être longue, à faible rendement et difficilement transposable à l’échelle industrielle.