macroflore benthique

LA MACROFLORE BENTHIQUE :
La macroflore benthique marine peut-être divisée en deux groupes : les macroalgues et les phanérogames marines. A la différence des macroalgues, les phanérogames marines sont des plantes à fleurs (aussi appelées Angiospermes ou Magnoliophytes), qui présentent des organes distincts, à savoir une tige, des feuilles et des racines. Ces plantes portent des fleurs puis des fruits.
En milieux côtiers, les phanérogames marines sont à l’origine de la création d’habitats particuliers, appelés herbiers, reconnus d’intérêt patrimonial majeur dans le cadre de Natura 2000 en mer. Un herbier est constitué par le regroupement d’une ou de plusieurs espèces de phanérogames marines, localisés généralement sur des sédiments meubles. Ces phanérogames sont constituées par des pousses végétatives et des pousses reproductives qui se développent le long d’un rhizome qui peut se trouver à la surface ou enfoui dans le sédiment, et duquel partent des racines qui s’enfoncent dans les couches plus profondes du substrat.
Il existe seulement une soixantaine d’espèces de phanérogames marines dans le monde, dont les principales sur les côtes européennes atlantiques sont : Zostera marina Linnaeus, 1753, Zostera noltei Hornemann, 1832, Ruppia maritima Linnaeus, 1753 et Ruppia cirrhosa (Petagna) Grande, 1918. Les zostères colonisent les habitats marins alors que les ruppies sont observées en milieux lagunaires. Il faut noter que Zostera marina et Zostera noltei sont respectivement classées CR (en danger critique) et EN (En danger) sur la liste rouge de l’UICN.
La dénomination « macroalgues marines » est usuelle mais regroupe de vraies plantes marines comme les algues rouges, Rhodophyta, et les algues vertes, Chlorophyta, ainsi que le groupe des Chromista ou algues brunes. Cette distinction est basée sur les caractéristiques de leurs organites photosynthétiques. Le long des côtes atlantiques françaises sont décrites environ 700 espèces de macroalgues alors que pour les Pertuis charentais, du fait de particularités biogéographiques et hydrologiques, moins de 340 espèces sont répertoriées, dont 2/3 d’algues rouges. Les macroalgues colonisent préférentiellement les substrats rocheux en s’organisant en ceintures algales, dont plusieurs sont nommées selon les espèces de Fucus, comme Fucus spiralis, Fucus vesiculosus ou Fucus serratus. De nombreuses espèces sont épiphytes (fixées sur d’autres algues) ou épizoaires (fixées sur d’autres animaux). Certaines macroalgues colonisent les substrats meubles (vasière, étier, lagune côtière, claire ostréicole) alors que, lors de marées vertes, certaines espèces de macroalgues vertes peuvent se développer de façon incontrôlée mais libres dans la colonne d’eau.
LA MACROFLORE BENTHIQUE ETUDIEE :
Les chercheurs de l’équipe BIOFEEL focalisent leurs recherches sur le fonctionnement des herbiers en zone intertidale, très largement dominés par l’espèce Zostera noltei. La particularité de cette espèce est qu’elle est le support de biomasses relativement faibles d’épiphytes, alors que les feuilles de phanérogames marines sont généralement couvertes par de grandes quantités de microalgues et de macroalgues épiphytes, celles-ci constituant alors une ressource trophique importante pour la faune qui colonise ces herbiers. Dans les herbiers intertidaux, les microalgues du sédiment (aussi appelées microphytobenthos) ont ainsi un rôle très important dans le fonctionnement de la chaîne alimentaire, alors que la matière issue des phanérogames marines est relativement peu exploitée par la faune. Ces herbiers de phanérogames marines jouent par contre un rôle important d’habitat pour la faune en relation avec la structure tridimensionnelle de l’habitat qu’elles créent.
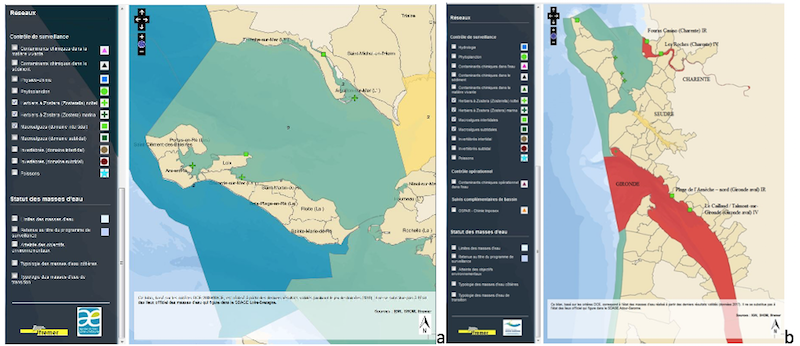
Les chercheurs de l’équipe BIOFEEL sont impliqués dans les programmes institutionnels de surveillance de la Directive Cadre sur l’Eau depuis sa mise en place sous l’égide d’Ifremer, du MNHN et des Agences de l’Eau Loire-Bretagne et Adour Garonne. La qualité des masses d’eau est évaluée selon un état chimique et un état biologique, ce dernier tient compte d’éléments de qualité biologiques dont font partie les Angiospermes ( Zostera marina et Zostera noltei) et les macroalgues de substrats rocheux et vaseux. Dans le périmètre des Pertuis charentais et de l’estuaire aval de la Gironde six sites pour les macroalgues et six sites pour les herbiers de Zostera noltei sont suivis.
LA RECHERCHE SUR LA MACROFLORE BENTHIQUE :
– Etude et quantification des flux de matière dans les herbiers intertidaux par utilisation de traceurs de la matière (isotopes stables, acides gras).
– Détermination de la structure des communautés de méiofaune et de macrofaune dans les herbiers.
– Taxinomie du genre Ulva par utilisation de marqueurs génétiques (ITS, rbcL, tufA, atpI-H, trnA-N) afin de caractériser la biogéographie et l’histoire de l’introduction d’une espèce comme Ulva australis Areschoug, 1854 et de déterminer le niveau spécifique d’espèces au sein du genre Ulva.
LES CHERCHEURS CONCERNES :
Fabien Aubert
Benoit Lebreton
Luuk van der Heijden
LES OUVRAGES DE REFERENCE :
- Ar Gall E., Le Duff M., 2007. Protocole d’observation in situ et proposition de calcul d’un indice de qualité pour le suivi des macroalgues sur les estrans intertidaux rocheux dans le cadre DCE. LEBHAM - IUEM – UBO, Brest, p. 14.
- Auby I., Oger-Jeanneret H., Gouillieux B., Grall J., Janson A.-L., Maguer M., Rigouin L., Rollet C., Sauriau P.-G., Trut G., 2018. Protocoles de suivi stationnel des herbiers à zostères pour la Directive Cadre sur l’Eau (DCE). Zostera marina - Zostera noltii. Version 3, REBENT réseau benthique. Ifremer, Arcachon, p. 63.
- Bréret M., 2008. Inventaire algologique des côtes charentaises 1976 - 2006 : 30 ans d’étude de la SBCO. Bulletin de la Société Botanique du Centre-Ouest, Nouvelle Série 39, 567-574.
- Brodie J.A., Maggs C.A., John D.M., 2007. Green seaweeds of Britain and Ireland. Dunmurry : British Phycological Society, London, 242 p.
- Burel T., Le Duff M., Ar Gall E., 2019. Updated check-list of the seaweeds of the French coasts, Channel and Atlantic Ocean. An aod – les cahiers naturalistes de l’Observatoire marin 7, 1-38.
- Green E.P., Short F.T., 2003. World atlas of seagrasses. University of California Press, Berkeley, 310 p.
- Larkum A.W.D., Orth R.J., Duarte C.M., 2006. Seagrasses : biology, ecology and conservation. Springer, Dordrecht, 691 p.
- Short F.T., Coles R.G., 2001. Global seagrass research methods. Elsevier, Amsterdam, 473 p.
PRINCIPALES PUBLICATIONS DE BIOFEEL :
- Lebreton B., Richard P., Radenac G., Bordes M., Bréret M., Arnaud C., Mornet F., Blanchard G.F., 2009. Are epiphytes a significant component of intertidal Zostera noltii beds ? Aquatic Botany 91, 82-90.
- Lebreton B., Richard P., Galois R., Radenac G., Pfléger C., Guillou G., Mornet F., Blanchard G.F., 2011. Trophic importance of diatoms in an intertidal Zostera noltii seagrass bed : Evidence from stable isotope and fatty acid analyses. Estuarine, Coastal and Shelf Science 92, 140-153.
- Lebreton B., Richard P., Galois R., Radenac G., Brahmia A., Colli G., Grouazel M., André C., Guillou G., Blanchard G.F., 2012. Food sources used by sediment meiofauna in an intertidal Zostera noltii seagrass bed : a seasonal stable isotope study. Marine Biology 159, 1537-1550.
- Robin F., Piersma T., Meunier F., Bocher P., 2013. Expansion into an herbivorous niche by a customary carnivore : black-tailed godwits feeding on rhizomes of Zostera at a newly established wintering site. The Condor 115, 340-347.
- Sauriau P.-G., Dartois M., Becquet V., Aubert F., Huet V., Bréret M., Viricel A., Pante E., 2021. Multiple genetic marker analysis challenges the introduction history of Ulva australis (Ulvales, Chlorophyta) along French coasts. Eurpean Journal of Phycology On line, 1-13.
- van der Heijden L.H., Graeve M., Asmus R., Rzeznik-Orignac J., Niquil N., Bernier Q., Guillou G., Asmus H., Lebreton B., 2019. Trophic importance of microphytobenthos and bacteria to meiofauna in soft-bottom intertidal habitats : a combined trophic marker approach. Marine Environmental Research 149, 50-66.
- van der Heijden L.H., Niquil N., Haraldsson M., Asmus R.M., Pacella S.R., Graeve M., Rzeznik-Orignac J., Asmus H., Saint-Béat B., Lebreton B., 2020. Quantitative food web modeling unravels the importance of the microphytobenthos-meiofauna pathway for a high trophic transfer by meiofauna in soft-bottom intertidal food webs. Ecological Modelling 430, 109129.




